Оксфордски университет
Доц. Лъчезар Карагьозов
Днес всяко лекарство, да не говорим за ваксина, преди да може да се използва широко, трябва да премине през сложна система от проверки.
Предклинични проверки
Да си представим, че един изследователски център или фармацевтична фирма искат да създадат ново лекарство. Научни публикации, собствени и чужди, проведените предварителни експерименти показват, че най-вероятно то ще помогне да се лекува по-добре някоя болест.
Но желанието да се въведе в лекарската практика ново лекарство, не е достатъчно. Преди всичко трябва да се докаже, че предложеното лечение не е опасно и няма да навреди. Задължително лекарството трябва да премине през тестове за токсичност. Primum non nocere, т.е. „Преди всичко не вреди“ – това е принцип, заложен в основата на лекарската професия още от времето на Хипократ.
Началните изпитвания трябва да бъдат проведени върху групи от две различни лабораторни животни – мишки, плъхове, зайци, морски свинчета, хамстери. Използват се различни дози от вещес-
твото, определя се как то се разпределя в организма, как и колко бързо се отделя. Наблюдава се състоянието на всички системи – кръвоносна, дихателна, опорно-двигателна, нервна. Следи се за промени в поведението. Тъй като това са животни с кратък размножителен период, следи се и за влиянието върху плода. В средата на миналия век на това не се е обръщало внимание, което в един от случаите е довело до нещастни последици.
Случаят „Талидомид“
Лекарството „Талидомид“ е било ново, предписвано е като леко успокоително и сънотворно. Употребявали са го и много жени в началото на своята бременност. Оказва се обаче, че „Талидомид“ влияе върху развитието на плода и може да предизвика различни вродени анатомични аномалии. Получава се трагедия – в света около десет хиляди деца са родени с физически недостатъци.
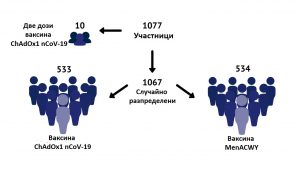
на оксфордската ваксина, втора фаза (схема)
Избрани са 1077 участници, дали писмено информирано съгласие. Десет от тях
получават последователно две дози от ваксината (ще бъде проверен техният имунен отговор). Останалите
на случаен принцип са разделени на две групи. Едната група – опитната, получава оксфордската ваксина ChAdOx1 nCov-19. Контролната група получава ваксината MenACWY срещу менингококи. Никой не е боледувал от Covid-19 или менингококи. Проверява се поносимостта на оксфордската ваксина
Подбор на участниците
Проучванията при хора могат да започнат едва след като опитите с лабораторни животни покажат, че лекарството няма вредно въздействие.
Отначало се подбират участниците, най-често доброволци. След това се разпределят по групи. Едната група е опитната – участниците в нея ще получат предполагаемото лечение. Другата група е контролната, спрямо нея ще се отчете ефектът от лечението. Участниците от контролната група не получават активното вещество.
В групите участниците трябва да са случайно разпределени; групите трябва да са рандомизирани. В никоя от групите не трябва да преобладават например жените или бол-
ните от диабет. Това се отнася и до други десетки показатели. Процесът на рандомизация е задължителен при провеждане на клиничните проверки.
Проверките – слепи, с плацебо
По време на проучванията участниците не трябва да знаят в коя група са – в опитната или в контролната. Те трябва да са „слепи“ за това. Ако знаят, че получават лекарство, може да започнат да се чувстват „добре“, ако вярват в него, или – „зле“, ако мислят, че то не става за нищо. Природата на човека е такава. Хората, и без да искат, се поддават на внушение. Самият факт, че ги лекуват, намалява тревогата, болката, подобрява настроението.
Ето защо при клиничните проучвания всеки участник е в неизвестност какво получава. Например той пие по една таблетка сутрин и вечер, но не знае дали получава лекарство, или плацебо. Плацебо прилича на даваното лекарство по външен вид, но няма съставката, за която се предполага, че лекува. Лекарството и неговото плацебо трябва да са неразличими по опаковка, форма, размери, цвят, вкус, миризма. Така се избягват разликите, които се дължат на така наречения „плацебо ефект“ – подобряване на самочувствието, което зависи от вярата в ефективността на прилаганото лечение. Положителният ефект на хомеопатичните лекарства се дължи на техният плацебо ефект.
Лекарите – също „слепи“
Не само участниците трябва да са „слепи“. Същото се отнася и до лекарите, които отчитат резултатите. Те не трябва да знаят дали изследваният, с когото разговарят и когото тестват, е от контролната или от
опитната група. Лекарят може несъзнателно да изрази отношение или да „мръдне“ малко резултата. Кой участник какъв е бил, ще стане ясно едва след завършване на проверката.
Това е златният стандарт на клиничните проверки: протоколът на изпитванията трябва да включва сравнение с плацебо, третиране на големи рандомизирани групи и двойно сляпо отчитане на ефектите.
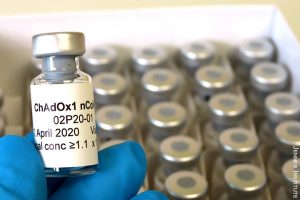
на Университета в Оксфорд
Клинични проверки – първите две фази
Клиничните проверки на лекарствата и ваксините преминават през три фази. През първите две фази се изследва безопасността на различните дози на лекарството или ваксината. Разработващите организации са задължени при всяка фаза да дават съобщения за пресата за проведените изследвания.
Ето какво е направено за ваксината срещу Covid-19 от Университета в Оксфорд и фармацевтичната фирма „Астра Зенека“. Ваксината е с техническото име ChAdOx1 nCoV-19; известна е още като AZD1222.
В края на март 2020 започва тестване на 1077 доб-
роволци от всички възрастови групи, някои от които са инжектирани с новата ваксина, а други – с „контролна ваксина“. Непосредствената реакция от ваксинирането се следи от самите участници и от лекари в течение на две-три седмици. За контрола е използвана друга, отдавна прилагана ваксина срещу менингококи, а не физиологичен разтвор. Така ще се разбере има ли разлика в реакцията на организма срещу двете ваксини.
През юли в списание „Лансет“ е публикуван крайният резултат. Накратко, оксфордската и старата ваксина се понасят еднакво добре; ChAdOx1 nCoV-19 води до силен имунен отговор, особено след две последователни дози. По всичко изглежда, че ваксината „Оксфорд“, прилагана правилно, ще дава защита срещу заболяване от Covid-19.
Третата фаза
С ваксината срещу новия коронавирус трябва да се бърза: независимо от мерките броят на заразените расте, броят на починалите – също. Икономиката на страните страда. След като са получени първите данни, потвърждаващи ефикасността на ваксината, от Оксфордската група започват изпитвания от фаза III. Те ще включват участници от най-различни места в няколко континента. Финансово това е най-скъпата част на клиничните проучвания. През юни е започнало ваксиниране във Великобритания, Южна Африка и Бразилия, което обхваща десетки хиляди участници. Първите резултати ще станат известни през септември или октомври.
Производство на ваксината
Оксфордската ваксина ще се произвежда от „Астра Зенека“ и други фирми, получили лиценз. Европейският съюз е подписал спогодба за получаването на 400 милиона дози с начало на доставката края на 2020. Трудност ще бъде да се организира ваксинирането на толкова много хора.

Уважаеми читатели, в. „Аз-буки“ и научните списания на издателството може да закупите от НИОН "Аз-буки":
Адрес: София 1113, бул. “Цариградско шосе” № 125, бл. 5
Телефон: 0700 18466
Е-mail: izdatelstvo.mon@azbuki.bg | azbuki@mon.bg